
Dentre a imensa variedade de materiais existentes, naturais e artificiais, o diamante é, provavelmente, aquele que mais desperta interesse, fascínio e cobiça. Esse fascínio está intimamente ligado às propriedades físicas extremas desse material, como sua altíssima dureza, a maior entre todos os materiais conhecidos. Essa característica inclusive inspira seu nome, que tem origem na palavra “adámas”, cujo significado no grego antigo é “indomável“ ou “invencível“. Além disso, os diamantes possuem uma dispersão de luz excepcional, ou seja, a capacidade de decompor a luz branca nas múltiplas cores do arco-íris, que é realçada quando são cortados, lapidados e polidos, aumentando seu brilho e resultando em um apelo visual incomparável (veja figura 1).
Além de suas propriedades excepcionais, a raridade de certas gemas lhes confere um valor extraordinário. O diamante natural mais caro já vendido, o Pink Star, um cristal rosa de 59,60 quilates1, por exemplo, foi arrematado por US$ 71,2 milhões em um leilão da Sotheby’s em Hong Kong, em abril de 2017.

Figura 1 – O Diamante Centenário de 273,85 quilates, um dos maiores diamantes lapidados do mundo (esq.) e o Pink Star, o diamante natural mais caro já vendido (dir.)
Alguns textos antigos eram categóricos sobre os poderes do diamante e deixavam claro que quanto melhor a qualidade da pedra, mais poderosa ela seria. O Garuda Purana, por exemplo, um texto sânscrito datado provavelmente do século IV ou V d.C., dizia “serpentes, tigres e ladrões fogem da presença de uma pessoa que usa tal diamante”. O fascínio por esta pedra preciosa levou, ao longo dos séculos, muitos a acreditarem que os diamantes, além do poder de proteger seu portador, também detinham propriedades místicas e podiam até mesmo promover a cura. Essa crença era tão forte que algumas pessoas chegaram a ingerir gemas na esperança de aliviar males do corpo e da alma. Curiosamente, uma outra propriedade no passado comumente atribuída ao diamante era sua eficácia como veneno. Entretanto, este mito não encontra nenhuma base concreta. Acredita-se que tenha sido criado e difundido como forma de desestimular os trabalhadores das minas a tentarem roubar gemas escondendo-as na boca ou deglutindo-as.
A despeito de toda aura em torno deste mineral, o diamante hoje encontra grande campo de aplicação no mundo concreto da indústria, como material abrasivo, em ferramentas de corte e furação, para usinagem de materiais muito duros e frágeis, como metais de alta resistência e materiais cerâmicos, ou na forma de pó para lixamento, polimento e lapidação de materiais duros e pedras preciosas. Na construção civil é utilizado em lâminas de serra e brocas para asfalto, concreto, granito e outras rochas, em brocas de perfuração na indústria de óleo e gás e também na odontologia (figura 2). Pode-se dizer sem exagero que o diamante é um material essencial para diversas áreas da indústria moderna.

Figura 2 – Ferramentas diamantadas. Graças às suas propriedades mecânicas excepcionais, os diamantes são materiais essenciais para um grande número de operações industriais, como corte, furação, usinagem, lixamento, polimento, lapidação, perfuração, etc.
O primeiro registro escrito conhecido sobre diamantes consta de um manuscrito em sânscrito do séc. IV a.C. encontrado na Índia, região que dominou a produção mundial destas pedras desde a história antiga até meados do séc. XVIII, quando novas jazidas foram descobertas no Brasil e mais tarde no séc. XIX na África do Sul.
Entretanto, achados arqueológicos surpreendentes realizados em 2005 indicam que diamantes já eram utilizados desde a Pré-História. O pesquisador P. J. Lu da Universidade de Harvard e seus colaboradores obtiveram evidências da utilização deste mineral para o polimento de machados de pedra pré-históricos encontrados na China. Um destes machados, datado de cerca de 2.500 a.C., composto em grande parte (40%) por corundum, um mineral natural extremamente duro à base de alumina (Al2O3), apresenta a superfície tão perfeitamente polida, que reflete imagens como um espelho. Os pesquisadores utilizaram técnicas modernas para reproduzir o polimento das superfícies de fragmentos destas rochas e posteriormente as investigaram em escala nanométrica com o auxílio da técnica de microscopia de força atômica (atomic force microscopy, AFM2). Esta análise permitiu concluir que a utilização de diamantes seria a única forma de obter um polimento com tal grau de perfeição e que, portanto, diamantes já eram utilizados na China há 4.500 anos!
Embora o diamante tenha sido utilizado já há séculos, o conhecimento de sua composição e estrutura é muito mais recente. O químico francês A. Lavoisier foi o primeiro a demonstrar em 1772 que o diamante é composto exclusivamente por carbono – assim como também é o grafite – após realizar sua combustão em atmosfera de oxigênio e obter apenas gás carbônico. Os átomos de carbono no diamante se organizam de forma que cada átomo esteja ligado a outros 4 átomos, formando tetraedros regulares que se organizam em uma estrutura de simetria cúbica. Pode-se entender essa estrutura de maneira simples: em uma célula cúbica (veja figura 3), os átomos de carbono ocupam os 8 vértices (bolas brancas) e os centros das 6 faces (bolas cinzentas) e 4 átomos (bolas pretas) no centro de cada tetraedro regular formado por 3 bolas cinzentas e uma bola branca.
A distância interatômica no diamante é muito pequena, apenas 0,1544 nm (1 nm = 10-9 m). Dessa maneira, sua densidade atômica (número de átomos por unidade de volume) é a maior dentre todos os materiais conhecidos. Essa estrutura extremamente densa, desvendada em 1913 por W. H. Bragg e seu filho W. L. Bragg, pouco após terem desenvolvido a técnica de difração de raios X, aliada a ligações interatômicas muito estáveis, são as bases das propriedades mecânicas excepcionais deste material.
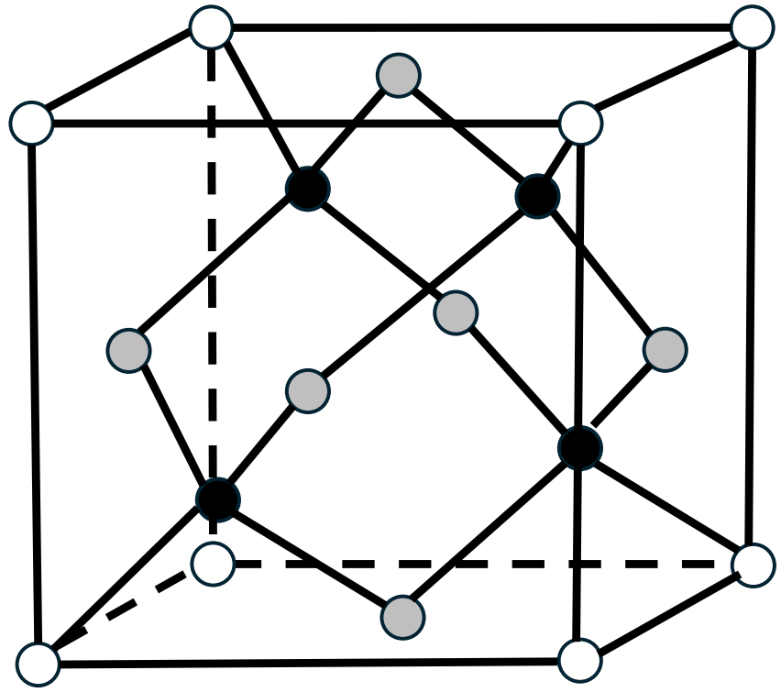
Figura 3 – A estrutura cristalina do diamante mostrando as ligações covalentes entre átomos de carbono formando tetraedros
Outra consequência dessa estrutura muito compacta é que os átomos de nitrogênio e boro, vizinhos do carbono na tabela periódica e, portanto, que apresentam raios atômicos próximos ao seu, são aqueles que normalmente se incorporam como impurezas no diamante natural, ocupando seu lugar na rede cristalina3. Outras impurezas não são encontradas com frequência neste mineral. Diamantes podem ocorrer na natureza como gemas de diferentes formas, como cubos, octaedros e dodecaedros, e de cores variadas. Em ordem de raridade crescente, podemos listar: amarelo, marrom, incolor, azul, verde, preto, rosa, laranja, roxo e vermelho.
Conforme foi dito acima, a estrutura cristalina do diamante foi esclarecida no início do século XX. No entanto, cientistas e gemólogos observaram que propriedades, como absorção de luz nas regiões do infravermelho e do ultravioleta, luminescência, fotocondutividade, além do próprio espectro de difração de raios X, apresentam diferenças entre os distintos tipos de gemas. Estas variações intrigaram os pesquisadores durante anos, levando alguns a propor até mesmo que os diamantes poderiam apresentar estruturas distintas com posições atômicas semelhantes, mas com diferentes orientações espaciais dos tetraedros de carbono. Um longo trabalho de pesquisa, desenvolvido principalmente entre as décadas de 1930 e 1950 foi necessário para decifrar o quebra cabeça dos diferentes tipos de diamante.
Atualmente está estabelecido um sistema de classificação de diamantes em duas categorias, cada uma delas subdividida em dois grupos. Esse sistema se baseia unicamente na presença ou ausência de impurezas (principalmente o nitrogênio, mas também o boro) no cristal e nas formas com que estas impurezas se arranjam na rede cristalina. Os diamantes que contêm nitrogênio em quantidades apreciáveis são do tipo I, enquanto os que contêm muito pouco nitrogênio são do tipo II. Os diamantes que contêm nitrogênio se dividem em dois subgrupos, aqueles onde os átomos de nitrogênio se encontram agrupados ou formando agregados (Ia) e aqueles onde esses átomos estão isolados uns dos outros (Ib). Os diamantes do tipo IIa, conforme dito acima, são aqueles que contêm muito pouco nitrogênio e, portanto, são os que mais se aproximam da estrutura cristalina perfeita. Os do tipo IIb, por outro lado, não contêm nitrogênio, porém contêm impurezas de boro.

Figura 4 – Os quatro tipos de diamante e suas diferentes cores (adaptado de 4)
A cor do diamante, assim como acontece nos demais materiais cristalinos isolantes, é fortemente influenciada pela presença de impurezas e defeitos na sua estrutura cristalina. Consequentemente, o tipo de diamante desempenha um papel importante na definição da cor das pedras, embora não exista uma correspondência simples e direta entre cor e tipo da gema (figura 4). Apenas um especialista é capaz de identificar o tipo do diamante por meio da simples inspeção visual. Os diferentes tipos de diamante em geral são distinguidos por meio da utilização da espectroscopia de absorção no infravermelho, embora outras técnicas também possam ser utilizadas. Mais detalhes sobre a classificação de diamantes podem ser encontrados na referência4.
Uma nova forma de diamante, de estrutura cristalina hexagonal, foi proposta em 1967 a partir da análise de amostras extraídas de meteoritos. Essa fase do diamante recebeu o nome de lonsdaleíta em homenagem à pesquisadora Kathleen Lonsdale que deu grandes contribuições para o avanço do conhecimento sobre a estrutura deste mineral. Muito rara, essa nova estrutura se formaria a partir da transformação do grafite induzida pela alta pressão resultante do choque de meteoritos com a superfície da Terra. Desde então, pode-se encontrar na literatura inúmeros trabalhos que reportam a identificação da lonsdaleíta em amostras não só de meteoritos, como também de sedimentos encontrados em locais associados a impactos de asteroides, bem como em uma diversidade de materiais de carbono sintetizados em laboratório pelas mais diversas técnicas. Um fato que atraiu atenção especial dos pesquisadores para este novo material é que cálculos computacionais indicaram que o diamante hexagonal, caso existisse, poderia superar as propriedades mecânicas do diamante convencional (de estrutura cúbica) em até 58%. Entretanto, este fato nunca pôde ser comprovado na prática uma vez que a lonsdaleíta até hoje não foi sintetizada.
Em anos recentes, entretanto, uma investigação mais profunda da estrutura dessas amostras mostrou que, na realidade, esses materiais não são constituídos por uma única estrutura cristalina hexagonal, como se acreditava anteriormente. São formados por uma complexa mistura desordenada de estruturas cúbica e hexagonal contendo defeitos e que, portanto, a lonsdaleíta enquanto fase cristalina do diamante de fato não existe.
O sonho de produzir diamantes artificiais levou muitos cientistas a se dedicarem a desenvolver diferentes métodos e processos para produzir esta forma de carbono sob condições controladas. Desde os primeiros experimentos que se têm notícia no século XIX, assim como aqueles realizados no início do século XX, todos obtiveram resultados negativos ou não comprovados. Em meados do século XX, entretanto, os diamantes artificiais se tornaram realidade, abrindo um novo campo de possibilidades de aplicações. Entretanto, a complexidade e os custos envolvidos nos processos de produção, bem como questões técnicas, impõem limitações sobre os produtos obtidos. Assim, hoje os diamantes artificiais disputam mercado com os naturais tanto no campo da joalheria, como para uma série de aplicações práticas, com uma participação que cresce continuamente. Com recursos naturais limitados e a tecnologia em constante desenvolvimento, espera-se que no futuro os diamantes artificiais venham a prevalecer.
Existem basicamente dois tipos de processos de produção: o de alta pressão e alta temperatura (high pressure and high temperature, HPHT); e a deposição química a vapor (chemical vapour deposition, CVD) a baixa pressão. Enquanto o método HPHT é mais utilizado para produzir diamantes industriais devido à sua eficiência em larga escala, o CVD é preferido para aplicações eletrônicas e ópticas, pois permite maior controle sobre as propriedades do material.
O diamante é produzido pelo processo HPHT desde a década de 1950, a partir do carbono sólido (grafite, p. ex.) em grandes prensas, a pressões da ordem de 5 a 6 GPa (50 a 60 mil atmosferas, aproximadamente) e temperaturas da ordem de 1.500 K a 2.000 K, que são condições nas quais o diamante é a fase mais estável do carbono. Nesse caso, é comum utilizar-se catalisadores para acelerar o processo de transformação do grafite em diamante (veja figura 5).

Figura 5 – Uma planta chinesa de produção de diamantes pelo processo HPHT
No processo CVD, desenvolvido na década de 1980, o diamante é produzido a partir de gases de hidrocarbonetos (metano ou acetileno, p. ex.), fortemente diluídos em hidrogênio, a pressões abaixo da pressão atmosférica e alta temperatura. Neste caso, o diamante se forma sobre um substrato sólido que deve ser constituído por um material refratário, uma vez que o processo ocorre em alta temperatura. A depender do tipo de aplicação o substrato posteriormente deve ser removido (ver figura 6).

Figura 6 – Exemplos de diamantes produzidos por CVD: uma joia lapidada de 16,41 quilates (esq.) e discos de diamante utilizados em diferentes aplicações (dir.)
Apesar de todas as suas vantagens, entretanto, o diamante é um material que tem uma resistência a impactos relativamente baixa e também é pouco deformável, o que limita muitas aplicações mecânicas. A despeito disso, atualmente é possível sintetizar pelo processo HPHT cristais com dureza superior ao dobro daquela do diamante convencional, aliada a um aumento da resistência à fratura e da capacidade de deformação, utilizando como precursores nanomateriais de carbono adequadamente selecionados. O aperfeiçoamento das prensas de alta pressão também permitiu que o HPHT se tornasse um método rápido e econômico de produção de pedras de alta qualidade para o mercado de joias. Entretanto, o processo HPHT tem a grande limitação de produzir diamantes apenas na forma de pedras ou grãos, restringindo severamente sua gama de aplicações.
Além das propriedades já mencionadas, o diamante possui ainda a maior faixa de transparência óptica e o mais alto índice de refração dentre todos os materiais transparentes, características que contribuem para o seu atraente brilho. Apresenta também um coeficiente de dilatação térmica extremamente pequeno e a mais alta velocidade de propagação de ondas sonoras. Apesar de ser um excelente isolante elétrico, esse material apresenta a maior condutividade térmica de toda a tabela periódica, superior à de todos os elementos metálicos ou não metálicos, fazendo com que seja ideal para a dissipação ou transmissão de calor. Em consequência disso, a condução de calor é uma das formas mais simples de se distinguir um diamante verdadeiro de pedras falsas ou imitações. É também um material inerte do ponto de vista químico, não reagindo com a maioria das substâncias corrosivas, sejam ácidas ou básicas. Além disso, apresenta excelente compatibilidade com o organismo humano, ou seja, é biocompatível5.
Com todas estas propriedades extremas é de se esperar que o diamante apresente aplicações em muitas outras áreas além da indústria mecânica e da joalheria. A deposição por CVD, capaz de produzir camadas de diamante com espessura de nanometros, mícrons ou mesmo milímetros, parece ser a técnica ideal para viabilizar essas aplicações. Assim, após a descoberta do processo CVD, a pesquisa e produção do diamante por esta técnica sofreu em todo mundo um crescimento tão vertiginoso, que o preço do quilate de uma fina camada deste material chegou no ano 2.000 a atingir menos de US$ 1,00!
Atualmente, são três as principais aplicações de alta tecnologia do diamante que estão em desenvolvimento. A primeira delas envolve seu uso como semicondutor. Embora a grande maioria dos diamantes seja excelente isolante elétrico, os diamantes azuis (tipo IIb), que contêm impurezas de boro, são semicondutores do tipo p. O boro substitui os átomos de carbono na rede cristalina, capturam um elétron e, portanto, criam buracos na banda de valência. Assim, verifica-se hoje um renovado interesse na produção de dispositivos eletrônicos (transistores) de diamante, aproveitando o grande desenvolvimento da técnica CVD.
A segunda aplicação está relacionada à utilização dos diamantes dopados com boro como eletrodos eletroquímicos de alto desempenho, permitindo uma gama de novas aplicações analíticas e como sensores. Por exemplo, estes eletrodos permitem realizar reações eletroquímicas em potenciais muito elevados (positivos e negativos) em meio aquoso, sem que o solvente seja decomposto; podem ser aplicados para tratamento de efluentes e águas residuais, na degradação eficiente de compostos orgânicos tóxicos e poluentes persistentes; como sensores de alta sensibilidade para detecção de metais pesados, fármacos, herbicidas e biomoléculas; ou como material de eletrodo superior de baterias devido à sua estabilidade contra a corrosão.
Finalmente, a terceira aplicação de alta tecnologia que tem atraído grande atenção em anos recentes utiliza certos defeitos cristalinos denominados centros nitrogênio-vacância (nitrogen vacancy, NV). Estes centros, que são constituídos por uma impureza de nitrogênio associada a uma vacância na rede cristalina6, apresentam luminescência, ou seja, emitem luz com comprimento de onda na região do vermelho. Os centros NV têm 3 estados distintos de spin: –1, zero e +17, que podem ser manipulados por campos elétricos ou magnéticos, radiação de micro-ondas ou incidência de luz, resultando em alterações na intensidade da luminescência. Dessa forma, os centros NV no diamante podem ser utilizados como sensores localizados em escala atômica. A utilização dos centros NV para a computação quântica também está sendo investigada intensamente.
Há cerca de dois mil anos, o escritor romano Plínio, o Velho, disse que o diamante era tão raro que seria um privilégio dos reis; um milênio depois, o escritor persa medieval al-Biruni escreveu que, entre as gemas, o diamante ocupava a posição equivalente à de um rei entre seus súditos. Dois milênios se passaram, e o diamante ainda parece ocupar o posto de rei dos materiais.
- O que equivale a 11,92 gramas, pois um quilate é igual a 0,2 gramas. ↩︎
- Para saber mais sobre a técnica AFM, clique aqui. ↩︎
- Quando um átomo estranho ocupa o lugar (substitui) outro na rede cristalina de um elemento ou composto, se diz que ele é uma impureza substitucional. ↩︎
- C. M. Breeding, J. E. Shigley, The “type” classification system of diamonds and its importance in gemology. Gems & Gemology 45 (2009) 96. ↩︎
- Para saber mais sobre as propriedades dos diamantes, consulte: S. S. Camargo Jr., Propriedades Físicas dos Materiais, Editora Blucher, São Paulo, 2024. ↩︎
- Uma vacância é um defeito que se caracteriza pela ausência de um átomo da rede cristalina. ↩︎
- O spin é uma propriedade fundamental da matéria, tal como a massa ou a carga, e não deve ser atribuído a um possível movimento de rotação. ↩︎
Deixe um comentário